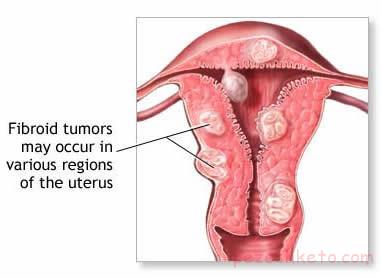
لیومیوسارکوم رحم یک تومور نادر ولیکن اگرسیو میباشد. معمولا با علایم خونریزی، درد و توده لگنی تظاهر میکند. درمان آن جراحی است. درمانهای کمکی تأثیری در سوروایوال بیماری تاکنون نداشتهاند. رادیوتراپی لگنی عود لگنی تومور را کم میکند ولیکن تأثیری در سوروایوال بیماری ندارد، شیمی درمانی نیز در افزایش سوروایوال بیماران به عنوان کمک درمانی در مراحل اولیه تأثیری نداشته است. در موارد پیشرفته و یا عود بیماری، از شیمی درمانی با استفاده از تاکسول+ کاربوپلاتین استفاده میشود. از جراحی در موارد متاستاز که رزکسیون تومور امکانپذیر باشد استفاده میشود. مطالعات جدید در مورد کاربرد روشهای درمانی بر اساس بیولوژی مولکولی در حال بررسی است.
 زمینه و هدف
زمینه و هدف
تومور عضله صاف رحم از میومتر رحم منشاء گرفته و شامل لیومیوم و لیومیوسارکوم میباشد. لیومیوم رحم یک تومور خوشخیم بوده و نسبتاً شایع میباشد به طوریکه در بعضی از جوامع تا 77% نیز گزارش شده است. در حالیکه لیومیوسارکوم یک تومور بدخیم با سیر تهاجمی و پیشآگهی بد بوده و نادر است و حدود 1 درصد کانسرهای رحمی را تشکیل میدهد. تظاهر بالینی هر دو این تومورها خونریزی رحمی، درد و علایم فشاری میباشد. لیومیوم معمولاً در دهه چهارم تا پنجم در حالی که لیومیوسارکوم در سنین بالاتر حدود دهه پنجم تا ششم زندگی میباشد. انسیدانس لیومیوسارکوم در نمونههای جراحی شده با تشخیص لیومیوم خیلی نادر است حدود 5/0% در حالی که هر چه سن بالاتر باشد و بیمار با علایم لیومیوم تحت جراحی قرار گیرد احتمال لیومیوسارکوم بیشتر و حدود 7/1% میباشد. گرچه همیشه عقیده بر این بوده که رشد سریع و ناگهانی لیومیوم احتمال سارکوم را بیشتر میکند ولیکن یک مطالعه مروری این عقیده را تأیید نمیکند. به طوریکه شانس سارکوم در لیومیومی که رشد سریع داشته است حدود 27/0% میباشد.1 بنابراین درمان لیومیوم رحم در زنان قبل از منوپوز ترجیحا محافظهکارانه میباشد و در صورت عدم پاسخ به درمانهای محافظهکارانه درمانهای جراحی پیشنهاد میشود.
ولیکن بروز یک توده رحمی پس از منوپوز، درمان جراحی را در اولویت قرار میدهد. لیومیوسارکوم رحمی توموری با پیشرفت تهاجمی و آگرسیو بوده و در موارد نادری پیشرفت کند دارد به طوریکه سوروایوال 5 ساله آن 75-25% میباشد.2 در این مقاله در مورد اپیدمیولوژی، نحوه مراقبت و درمان لیومیوسارکوم بحث خواهیم کرد.
اپیدمیولوژی و تظاهرات بالینی
1% تومورهای رحمی را لیومیوسارکوم رحم تشکیل میدهد. بیماران در سنین 60-50 ساله هستند. رادیوتراپی لگنی انسیدانس کارسینوسارکوم را افزایش میدهد (M.M.T) ولیکن رابطهای بین لیومیوسارکوم و رادیوتراپی وجود ندارد.4و3 همچنین مصرف تاموکسیفن شانس کارسینوسارکوم را افزایش میدهد نه لیومیوسارکوم را. علایم بیماری نیز خونریزی- درد و توده لگنی میباشد.5
آمبولیزاسیون شریان رحمی Uterine artery embolization
از سال 1995 که آمبولیزاسیون شریان رحمی (UAE) به عنوان روشی برای حفظ رحم در موارد لیومیومهای علامتدار، معرفی شد روز به روز محبوبیت بیشتری پیدا کرده است این روش توسط رادیولوژیستهای دوره دیده انجام میشود و از بین رفتن علایم بیماری و دوره نقاهت خیلی سریع بوده ولیکن چون نمونه پاتولوژی وجود ندارد ممکن است تشخیص LMS (لیومیوسارکوم) به تعویق بیافتد.6
جهت تشخیص LMS رحم قبل از انجام آمبولیزاسیون روش موثری وجود ندارد. انجام تستهای خونی، رادیولوژی و یا نمونهگیری از آندومتر کافی نمیباشند این بررسیها قبل از آمبولیزاسیون انجام میشود که میزان موفقیت درمانی را پیشبینی کند.9-7 انجام MRI قبل از آمبولیزاسیون بهترین روش برای تعیین موقعیت فیبروم میباشد زیرا فیبرومهای پدانکوله و سابسروز کمتر به این روش درمانی پاسخ میدهند.10 از طرفی سیگنالهای MRI تا حدودی ممکن است بتواند موارد بدخیم را نشان دهد.10 گرچه احتمال لیومیوسارکوم رحم در نمونههای جراحی برای لیومیوم خیلی کم میباشد (5/0%). ولیکن به هر حال وجود دارد و تاکنون هفت مورد لیومیوسارکوم رحم پس از آمبولیزاسیون گزارش شده است.12و11
که در سه مورد تأخیر در تشخیص شش ماه و در چهار مورد 12 ماه یا بیشتر بوده است. از این هفت مورد دو مورد متأسفانه در موقع تشخیص متاستاز داشتند. به هر حال آمبولیزاسیون رحمی یک روش مفید در درمان لیومیوم رحم می باشد. آمبولیزاسیون رحم در زنان پس از یائسگی پیشنهاد نمی شود و همچنین در بیماری که آمبولیزاسیون منجر به از بین رفتن علایم بیمار نمیشود و در حقیقت شکست درمانی وجود دارد این احتمال را باید در نظر گرفت و بیماران را برای جراحی کاندید کرد.
پاتولوژی
به طور کلی لیومیوسارکوم یک توده صاف، زردرنگ با نقاط نکروز و هموراژی میباشد. معمولا تشخیص هیستوپاتولوژیک لیومیوسارکوم مشکل نمیباشد و اکثر تومورهای بدخیم عضله صاف رحم دارای خصوصیات زیر هستند.
هیپرسلولاریتی، آتیپیسم هسته، میتوز بالا بیش از 15 میتوز در هر میدان میکروسکوپی (MF/10HPF) و علاوه بر آن معمولا ویژگیهای دیگر مثل منوپوز، گسترش تومور به خارج از رحم، سایز بزرگ (بیش از 10 سانتیمتر)، تهاجم تومور به نسوج اطراف، نکروز و آتیپیکال میتوز دیده میشود.
در مورد لیومیوسارکوم از نوع اپیتلوئید یا میگزوئید ممکن است تشخیص مشکل باشد زیرا آتیپیسم در هسته و تعداد میتوز کم است که در غیاب هیپرسلولاریتی و آتیپسم هسته معمولا این نوع لیومیوسارکوم بر اساس حاشیه تهاجمی تومور (Infiltrative border) تشخیص داده میشود.
گاهی تشخیص افتراق لیومیوسارکوم از نوع تومور عضله صاف و stump مشکل است. (جدول 2 و 3). اکثر پاتولوژیستها معتقدند در صورت دو معیار از سه معیار زیر تشخیص لیومیوسارکوم داده میشود:
– تعداد میتوز بیش از 10
– آتیپی سلولی
– وجود نکروز Coagulative necrosis
اکثر پاتولوژیستها وقتی دو تا از معیارهای فوق وجود داشته باشد تشخیص LMS میدهند. همانطور که گفته شد تشخیص افتراقی لیومیوم از لیومیوسارکوم ساده است و مشکلی در گزارش نهایی پاتولوژی وجود ندارد ولیکن در بعضی از لیومیومها گزارشاتی مثل آتیپیکال، سلولار، میتوتیک اکتیویتی و یا Bizarre leiomyoma وجود دارد که به شرح آنها خواهیم پرداخت.
Table- 1: Benign smooth muscle tumors of the uterus
Leiomyoma variants that may mimic malignancy Smooth muscle proliferations with unusual growth patients
Mtotically active leiomyoma Disseminated peritoneal leiomyomatosis
Cellular leiomyoma Benign metastasizing leiomoyoma
Hemorrhagic leiomyoma and hormone- induced changes Intravenous leiomyomatosis
Leiomyoma with bizarre nuclei (atypical leiomyoma) lymphangioleiomyomatosis
Myxoid leiomyoma
Epithelioid leiomyoma
Leiomyoma with massive lymphoid infutration
Table- 2: smooth muscle tumors of uncertain malingnat potential (STUMP)
Pathologic criteria
Tumor cell necrosis in a typical leiomyoma
Necrosis of uncertain type with≥10 MF/10 HPFs, or marked diffuse atypia
Marked diffuse or focal atypia with borderline mitotic counts
Necrosis difficult to classify
گزارشات دیگری مثل هیدورپیک لیومیوما، میگزوئید لیومیوما، اپیتلیوئید لیوموما، نیز وجود دارد.
Atypical leiomyoma آتیپی سلولی وجود دارد ولیکن نکروز دیده نمیشود. نوع شدید آتیپیکال لیومیوم همان bizarre میباشد که آتیپی سلول شدید است ولیکن علیرغم هیپرسلولاریتی تعداد میتوز از 10 عدد کمتر است و نکروز سلولی وجود ندارد.14و13
Kempson و Hendrickson یک گروه کوچک از تومورهای عضله صاف رحم (Smooth muscle tumors) را معرفی کردند که رفتار کلینیکی آنها را نمیتوان پیشبینی کرد این محققین از واژه Smooth muscle Tumors of Uncertain Malignant Potential (STUMP) برای آنها استفاده کردند.14
این تومورها شامل:
– تومورهای عضله صاف با حداقل آتیپیسم سلولی و تعداد میتوز کم ولیکن نمیتوان هیستولوژی آن را مشخص کرد.
– تومور عضله صاف با آتیپی سلولی منتشر و شدید، میتوز کم و عدم قطعیت در مورد وجود یا عدم وجود کوآگولاتیو نکروزیس
– تومور عضله صاف با میزان متوسط تا شدید آتیپی سلول و ایندکس میتوز که نمیتـوان قطعا تعداد آن را مشخص کرد به دلیل آن که احتمالا تعدادی از سلولهای در حال دژنراسیون شبیه به میتوز به نظر میرسد.
ایمونوهیستوشیمی Immunohistochemistry
لیومیوسارکوم معمولا مارکرهای عضله صاف را مثل h-caldesmon, desminT smooth- muscleactine، histone deactylase 8 را بیان میکند و بایستی بدانیم که نوع میگزوئید و اپیتلیوئید ممکن است برای این مارکرها مثبت نشود. همچنین لیومیوسارکوم CD10 و مارکرهای اپیتلیوئید مثل کراتین یا EMA را ممکن است بیان کند. لیومیوسارکومها ممکن است برای گیرندههای استروژن و پروژسترون هم مثبت شوند در مطالعات اخیر نشان داده شده که Ki67 نیز در سطح بالایی مثبت میشود.
فاکتورهای پروگنوستیک
لیومیوسارکوم رحم حتی اگر محدود به رحم باشد پیشآگهی بدی دارد در اکثر بیماران (40%) اولین عود در ریهها دیده میشود و در 13% عود ابتدا در لگن اتفاق میافتد. سوروایوال 5 ساله در بیماران در مرحله I، 50% و در مرحله II، 25% میباشد.
در مطالعات مختلف عوامل پیشآگهی شامل سن، سایز تومور، مرحله بیماری، حاشیه تومور، وجود یا عدم وجود نکروز، تعداد میتوز، میزان آتیپیسم سلولی و تهاجم به عروق، بوده است ولیکن توافق کلی در این زمینه وجود ندارد. یک مطالعه نشان داد که سایز تومور مهمترین عامل پروگنوستیک میباشد. در بعضی مطالعات دیگر سایر تومور و تعداد میتوز در تعیین پیشآگهی بیماری مهم بودهاند.
اکثرا معتقدند سایر پارامترها، عوامل وابسته به سایز تومور هستند و لذا اندازه تومور در staging جدید FIGO به عنوان یک عامل مهم در تعیین مرحله بیماری و بالطبع پیشآگهی آن آمده است.
جراحی Surgical management
خوشبختانه اکثر موارد تومورهای علامتدار رحمی که جراحی میشوند نهایتا هم خوشخیم هستند و فقط5/0% نمونههای هیسترکتومی ممکن است جواب لیومیوسارکوم باشد. همانطور که قبلا نیز گفته شد روش قطعی برای افتراق این دو پدیده خوشخیم و بدخیم قبل از جراحی وجود ندارد. نمونهگیری از آندومتر فقط در مواردی که توده سابموکوزال باشد ممکن است کمککننده باشد، MRI و اندازهگیری لاکتات دهیدروژناز گرچه کمک کننده هستند ولیکن قطعی نیست. برای Staging لیومیوسارکوم سیستم مرحلهبندی FIGO را باید به کار برد.15 تومور بایستی به طور کامل خارج شود. از روش میومکتومی در مواردی که بیمار حفظ باروری برایش مهم است و فرزند ندارد فقط هشت مورد گزارش شده است16 که وقتی به پاتولوژی این بیماران دقت میکنیم تعدادی از آنها لیومیومهای غیرعادی بوده است و در حقیقت سارکوم نبوده است. هیسترکتومی درمان استاندارد برای این بیماران میباشد.
حفظ تخمدانها
برای حفظ تخمدانها در بیماران مبتلا به لیومیوسارکوم رحم هنـوز جـواب قاطعـی وجود ندارد بعضی از سارکومهای رحمی
Table- 3: uterine sarcoma
Stage IA Tumor limited to uterus<5cm
Stage IB Tumor limited to uterus>5cm
Stage IIA Tumor extends to the pelvis, aderiexa
Stage IIB Tumor extends to extra- uterine pelvic tissue
Stage II1A Tumor extends to abdominal tissue one site
Stage IIIB More than one site
Stage IIIC Metastasis to pelvic and/or para- aortic lymphnode
Stage IV A Tumor inades bladder and/or rectum
Stage IV B Distant metastasis
گیرنده هورمونی دارند و همچنین احتمال متاستاز میکروسکوپی در تخمدان وجود دارد لذا حفظ تخمدانها مورد بحث است و یا قاطعیت نمی توان به آن پاسخ داد. در چندین مطالعه محققین وجود گیرندههای استروژنی را در لیومیوسارکوم گزارش دادهاند.18و17 همچنین در یک گزارش موردی، قطع استروژن پس از اووفرکتومی منجر به از بین رفتن متاستازهای ریه در بیمار لیومیوسارکوم با گرید پایین شد.19 بنابراین بر اساس این گزارشات این احتمال وجود دارد که با حفظ تخمدانها، سلولهای باقیمانده سارکوم ممکن است مجدداً رشد و منجر به عود بیمار میشوند. در چندین مطالعه نیز احتمال متاستاز مخفی در تخمدانها بررسی شده است در دو گزارش محققین گزارش کردهاند که در تخمدانها بهظاهر سالم در نمونه پاتولوژی نیز هیچ متاستازی مشاهده نشد.20
اما در گزارش دیگری از Levirao و همکارانش در 108 نمونه لیومیوسارکوم که تخمدانها به طور ماکروسکپی سالم بودند در 9/1% از بیماران (2 درصد) متاستاز در نمونه میکروسکپی مشاهده شد.21
بنابراین با در نظر گرفتن احتمال پایین درگیری تخمدان در تخمدانهایی که به ظاهر سالم هستند، حفظ تخمدانها در زنان جوان امکانپذیر است.
Aaro و همکارانشان سوروایول 5 ساله در 9 مورد لیومیوم سارکوم رحم با حفظ تخمدانها را 78% گزارش دادند.
مطالعات بعدی هم این نظریه را تأیید کردند.23و22 به طوری که در یک گزارش از میوکلینیک در 25 موردی که تخمدانها حفظ شد نسبت به بیماران که تخمدانها برداشته شده بود و از نظر stage، گرید و سن با هم مطابقت داشتند میزان عود و سوروایول تفاوتی نداشت.
با بررسی گزارش 1396 مورد لیومیوسارکوم محدود به رحم در 341 بیمار کمتر از 50 سال 5- year disease free survival در بیمارانی که اووفورکتومی شده بودند با آنهایی که اووفرکتومی شده بودند تفاوتی مشاهده نشد.24
لنفادنکتومی Lymph node evaluation
نقش لنفادنکتومی در لیومیوسارکوم رحم (LMS) مورد بحث است. در بررسی EER database در 348 مورد لیومیوسارکوم رحم 23 مورد (6/6%) غدد لنفاوی درگیر بود24 و سوروایول 5 ساله در آنهایی که غدد درگیر داشتند 26% نسبت به 64% در آنهایی که درگیری غدد نداشتند (001/0p<) ولیکن خود غدد لنفاوی درگیر به تنهایی تأثیری در سوروایول نداشت.7 در یک مطالعه توسط Gynecologic Oncology Group (GOG) در سارکوم رحم درگیری غدد لنفاوی تأثیری در پیشآگهی بیماری نداشت.25
به هر حال اینکه بررسی غدد لنفاوی در لیومیوسارکوم رحم لازم است یا نه. جواب قاطعی وجود ندارد ولیکن به نظر میرسد درگیری غدد لنفاوی در موارد پیشرفته بیماری دیده میشود و به همین دلیل پیشآگهی بیماری در این موارد بد میشود و اما در موارد نادری نیز گزارش شده است که در بیماری محدود به رحم، غدد لنفاوی درگیر بوده است.
شاخصهای پیشآگهی
همانطور که قبلا نیز گفته شد لیومیوسارکوم رحم یک بیماری تهاجمی با پروگنوز بد میباشد به طوریکه متوسط دوره عادی از بیماری پس از درمان 2/2 سال میباشد و متوسط سوروایوال 9/4 سال است.23
فاکتورهای موثر در پیشآگهی بیماری: گرید تومور، مرحله بیماری و تعداد میتوز میباشد.26
مروری بر یافتههای SEER data base نشان میدهد که سوروایول 5 ساله بیماران در مرحله I، II، III، IV به ترتیب 75%، 60%، 44% و 28% میباشد.24
سایر فاکتورها مثل سایز کوچک تومور، سن پایین، قبل از یائسگی عوامل موثر در پروگنوز خوب بیماری هستند در یک مطالعه اخیر نیز عدم درگیری فضاهای عروقی (Vascular space involvement) در پیشآگهی بهتر موثر بوده است.27و26
درمانهای کمکی Adjuvant therapy
رادیوتراپی
استفاده از رادیوتراپی در درمان لیومیوسارکوم رحم معلوم نیست. در یک بررسی مروری بر نتایج مطالعات که توسط sala zar و Dunne انجام شد تفاوتی در سوروایوال بیماران در مرحله I که رادیوتراپی گرفته بودند با آنهایی که دریافت نکرده بودند، مشاهده نشد.28 در بعضی از مطالعات نشان داده شده است که کنترل موضعی با رادیوتراپی بهتر میشود.29و25و23و22 در مطالعه Brooks و همکارانش در روی 2677 بیمار با سارکوم رحم اضافه کردن رادیوتراپی به جراحی در بیماران مرحله II-IV با سوروایول بهتر بیماران همراه بود. منتهی محققین در مورد هیستولوژی و باقیمانده تومور پس از جراحی صحبتی نکردهاند. تنها در یک مطالعه Randomized Trial (RCT) که 224 بیمار مرحله I و II سارکوم رحم (103 مورد LMS و 91 مورد کارسینوسارکوم و 28 مورد آندومتریال استرومال سارکوم) به دو گروه رادیوتراپی و بدون رادیوتراپی تقسیم شدند.30 در این مطالعات بیماران مبتلا به LMS با دریافت رادیوتراپی بهبودی در کنترل موضعی و بقا مشاهده نشد. محققین نتیجه گرفتند که تمایل LMS به متاستاز از راه خونی دلیل عدم پاسخ به رادیوتراپی و عدم بهبود میزان بقای بیماران میباشد. محققین مسیر کلینیک نیز با بررسی پرونده های بیماران همین نتیجه را گرفتند که رادیوتراپی تأثیری در میزان بقای بیماران ندارد.23 بنابراین رادیوتراپی کمکی پس از جراحی به بیماران توصیه نمی شود.
شیمی درمانی Adjuvant chemotherapy
مطالعه کنترل شده تصادفی (RCT) در مورد کاربرد شیمی درمانی به عنوان درمان کمکی (Adjuvant) در LMS رحم وجود ندارد.
داکسیروبین (Doxirubin) به عنوان موثرترین دارو معرفی شده است.33-31 Omura و همکارانش یک مطالعه RCT را در نقش کموتراپی کمکی مورد سارکوم رحم گزارش دادند در این مطالعه در سابگروههای مرحله I و II لیومیوسارکوم رحم تفاوتی در میزان عود در کسانی که شیمی درمانی گرفته بودند با آنهایی که درمانی نگرفته بودند مشاهده نشد. در مطالعه میوکلینیک نیز تفاوتی در سوروایول بیمارانی که شیمی درمانی دریافت کرده بودند با آنهایی که فقط کنترل شدند مشاهده نشد.23
رژیم ترکیب Gemcitabine به همراه Docetaxeol
نتایج قابل توجهی در بیماران متاستاتیک و عود نشان داده است. این رژیم اخیراً در 25 بیمار مرحله I-IV لیومیوسارکوم به کار رفته است.36و35 مدت زمان عاری از بیماری P.F.S در گروه درمان شده نسبت به گروه با درمانهای قبلی بیشتر بود.37 بنابراین هنوز تحقیقات در مورد لیومیوسارکوم و شیمی درمانی باید ادامه یابد. یک داروی جدید که نتایج رضایتبخشی نشان داده Trabectedine میباشد. یک نوع الکالوئید از گیاهان دریایی که باعث صدمه به DNA شود.38 گرچه هنوز مطالعه کافی در مورد آن وجود ندارد. یک گزارش اخیراً 45% پاسخ درمانی در زنان مبتلا به LMS که با رژیمهای دیگر درمان شده و پاسخ نداده بودند، دیدهاند. گرچه تعداد نمونه کم است ولیکن نتایج قابل توجه است.
عود Persistent or recurrent
در حدود 30% لیومیوسارکومها در موقع تشخیص متاستاز دارند (stage III, IV)24 و احتمال عود در LMS در حدود 40 تا 73 درصد میباشد. برای این بیماران درمانها مختلفی پیشنهاد میشود که شامل: جراحی مجدد و برداشتن تومور، شیمی درمانی، هورمون تراپی و درمانهای تسکینی (Palliative) میباشد. شیمی درمانی رایجترین درمانی است که در موارد عود بیماری به کار میرود Doxorubicine در حدود 25% پاسخ درمانی میدهد.33-31
یک مطالعه اخیرا با استفاده از Doxil (tiposomal doxorubicin) در موارد عود یا بیماری پیشرفته هیچ مزیتی نسبت به دوکسی روبین مشاهده نشد.40 اخیرا دو رژیم شیمی درمانی با نتایج قابل توجه در مورد عود لیومیوسارکوم معرفی شدهاند یکی از این رژیمها بهکارگیری Temozolomide و دیگری ترکیب Gemcitabin Docetaxel میباشد.
Temozolomide در بیماران با عود به خوبی تحمل شده و در 19 بیماری که به کار رفته است در دو مورد پاسخ و در بقیه پیشرفت بیماری متوقف شده است (stable).41
در مطالعه دیگری توسط Garcia و همکارانش پاسخ به Temozolomide در 5 بیمار از 11 بیمار مورد مطالعه دیده شد که مدت متوسط پاسخ به درمان 5/12 ماه (mm58-8/3) بوده است.42 ترکیب دیگر درمانی در موارد عود gemcitabine doxetaxol میباشد که Hensely با به کارگیری این رژیم به میزان mg/m2900 gemcitabine به همراه mg/m2100 Decetaxol به عنوان خط اول درمانی در بیماران 8/4% پاسخ کامل 35% پاسخ نسبی و در 26% پیشرفت بیماری متوقف شد.36 مدت متوسط پاسخ به درمانی 16 ماه بوده است. در یک مطالعه دیگر نیز در لیومیوسارکومهای رحمی که غیرقابل جراحی بودند و به شیمی درمانیهای قبلی پاسخ نداده بودند با این رژیم 27% پاسخ کامل و 20% پاسخ نسبی دیده شد.37
یکی دیگر از روشهای درمانی در بیماران دچار عود جراحی میباشد. رزکسیون متاستاز ایزوله ریوی در لیومیوسارکوم رحم با سوروایوال 5 ساله 40 درصد گزارش شده است.44و43 همچنین گزارش میوکلینیک نشان میدهد که جراحی cytoreductive در عود لیومیوسارکوم با پروگنوز بهتری همراه بوده است.45 با در نظر گرفتن نتایج این مطالعات به نظر میرسد جراحی در موارد عود که تومور قابل رزکسیون باشد در سوروایوال این بیماران موثر است. هورمون تراپی در لیومیوسارکوم پیشرفته یا عود به کار رفته است. تعدادی از تومورهای دستگاه ژنیتال از آن جمله LMS دارای رسپتور استروژن و پروژسترون هستند ولیکن درصد محدودی از این تومورها به هورمونتراپی پاسخ میدهند.
Akhan و همکارانش رسپتور استروژن Ki-67 و p53 را بررسی کردند و مشاهده کردند که سوروایول بیماران با بیش از 10% گیرنده استروژن و Ki-67 بهتر است.46 اخیرا یک مطالعه کیس- رپورت با استفاده از مهارکننده های آروماتاز در بیماران با رسپتور استروژن مثبت در بیمار LMS که دچار عود تومور در ریه شده بود تومور از بین رفت و پاسخ درمان برای 12 ماه باقی ماند.47
همانطور که قبلا هم گفته شد پس رفت بیماری پس از اووفرکتومی هم گزارش شده است.19 به هر حال جایگاه هورمونتراپی در LMS بایستی با مطالعات بیشتر مشخص تر شود. رادیوتراپی در عود لیومیوسارکوم اثرات بسیار محدودی در سوروایول دارد. رادیوتراپی در این موارد بیشتر نقش Palliative دارد. ضرورت دستیابی به درمانهای جدید در مورد LMS به شدت احساس میشود.
Molecular biology
Tyrosine kinase receptore: رسپتور تیروزین کیناز که برای پروتو انکوژن c-kit کد می شود در حقیقت یک تنظیم کننده پرولیفراسیون یا مرگ سلولی است و دیده شده در سرطانهای خونی، دیس ژرمینوما و سمینوما و تومورهای استرومال دستگاه گوارش (Gastagional stromal tumor) این رسپتورها وجود دارد. به همین دلیل درمان مهارکنندههای تیروزین کیناز مثل Imatinib در آنها خیلی موثر بوده است.48 متأسفانه مطالعات در روی LMS برای بررسی این رسپتور نتیجه مشخصی را نداده است و به نظر نمیرسد مهارکنندههای تیروزین کیناز در مورد لیومیوسارکوم موثر باشد.53-49
Matrix metalloproteinases: این مواد در حقیقت مواد خارج سلولی هستند که در تهاجم سلولی و ایجاد متاستاز موثر هستند (MMPs). مطالعاتی نشان داده است که MMP در 86% لیومیوسارکوم مثبت است و آن دسته از LMS که فاقد MMPs هستند رشد بطئی و غیرتهاجمی دارند.54
همچنین ممکن است با بررسی Tissue- Microarray بتوان تقسیمبندی جدیدی برای لیومیوسارکوم درست کرد.56و55
با استفاده از Microarray– analysis ممکن است اطلاعات بیشتری از تغییرات مولکولار در سلولهای سرطانی بهدست آورد به طوریکه مطالعات جدید نشان داده که ژن CDKIN2A و diaphanous در لیومیوسارکوم دچار تغییرات میشوند (upregulation) و با فهم بهتر این تغییرات ژنی می توان امیدوار بود که درمانهای بهتری برای سارکوم به وجود خواهد آمد (targeted therapy).
نتیجهگیری
لیومیوسارکوم رحم یک بیماری نادر و مهاجم میباشد. شیوع آن با افزایش سن بیشتر میشود. وجود یک توده رحمی علامتدار در یک خانم پس از منوپوز الزام بررسی دقیق و احتمالا جراحی را میطلبد. جراحی در لیومیوسارکوم رحمی شامل برداشتی کامل رحم همراه تخمدانها میباشد. حفظ تخمدانهای به ظاهر سالم در خانمهای جوان امکانپذیر است. ولیکن احتمال میکرومتاستاز و یا تأثیر هورمون استروژن در سیر بیماری را بایستی در نظر داشت. لنفادنکتومی یک روش پروگنوستیک است به هر حال در موارد نادری لنفنودها مثبت است مگر اینکه بزرگ باشند و یا بیماری در خارج از رحم وجود داشته باشد.درمانهای کمکی تأثیر در پروگنوز بیماری در مراحل اولیه (I, II) ندارد.
متأسفانه عود شایع است. Dexorobicin یک داروی قدیمی و موثر در موارد عود است. اخیراً رژیم Gemcitabine+ Decitaxol تأثیر قابل توجهی در موارد پیشرفته و عود داشته است. جراحی مجدد و رزکسیون تومور در بیمارانی که به خوبی انتخاب شوند روش مفیدی است. رادیوتراپی به عنوان درمان palliative موثر است. به نظر میرسد با پیشرفتهایی که در زمینه بیولوژی تومور در حال انجام است دسترسی به درمانهای جدید و موثرتر امکانپذیر خواهد بود.
منابع :
1. Cramer SF, Patel A. The frequency of uterine leiomyomas. Am. J. Clin. Pathol.94,435-438 (1990).
2. Harlow BL, Weiss NS, Lofton S. The epidemiology of sarcomas of the uterus. J. Natl Cancer Inst.76,399-402 (1986).
3. Leibsohn S, d’Ablaing G, Mishell DR Jr. Schlaerth JB. Leiomyosarcoma in a series of hysterectomies performed for presumed uterine leiomyomas. Am. J. Obstet. Gynecol.162,968-974 (1990).
4. Parker WH, Fu YS, Berek JS. Uterine sarcoma in patients operated on for presumed leiomyoma and rapidly growing leiomyoma. Obstet. Gynecol.83,414-418 (1994).
5. Aaro LA, Symmonds RE, Dockerty MB. Sarcoma of the uterus. A clinical and pathologic study of 177 cases. Am. J. Obstet. Gynecol.94,101-109 (1966).
6. Gard GB, Mulvany NJ, Quinn MA. Management of uterine leiomyosarcoma in Australia. Aust. NZ J. Obstet. Gynaecol.39,93-98 (1999).
7. Hannigan EV, Gomez LG. Uterine leiomyosarcoma. Am. J. Obstet. Gynecol.134,557-564 (1979).
8. Major FJ, Blessing JA, Silverberg SG et al. Prognostic factors in early-stage uterine sarcoma. A Gynecologic Oncology Group study. Cancer71,1702-1709 (1993).
9. Mayerhofer K, Obermair A, Windbichler G et al. Leiomyosarcoma of the uterus, a clinicopathologic multicenter study of 71 cases. Gynecol. Oncol.4,196-201 (1999).
10. Peters WA 3rd, Kumar NB, Fleming WP, Morley GW. Prognostic features of sarcomas and mixed tumors of the endometrium. Obstet. Gynecol.3,550-556 (1984).
11. Van Dinh T, Woodruff JD. Leiomyosarcoma of the uterus. Am. J. Obstet. Gynecol.144,817-823 (1982).
12. Jemal A, Siegel R, Ward E et al. Cancer statistics, 2008. CA Cancer J. Clin.58,71-96 (2008).
13. Brooks SE, Zhan M, Cote T, Baquet CR. Surveillance, epidemiology, and end results analysis of 2677 cases of uterine sarcoma 1989-1999. Gynecol. Oncol.93,204-208 (2004).
14. George M, Pejovic MH, Kramar A. Uterine sarcomas, prognostic factors and treatment modalities – study on 209 patients. Gynecol. Oncol.24,58-67 (1986).
15. Curtis RE, Freedman DM, Sherman ME, Fraumeni JF Jr. Risk of malignant mixed mullerian tumors after tamoxifen therapy for breast cancer. J. Natl Cancer Inst.96,70-74 (2004).
16. American College of Obstetricians and Gynecologists. ACOG practice bulletin. Alternatives to hysterectomy in the management of leiomyomas. Obstet. Gynecol.112,387-400 (2008).
17. Goto A, Takeuchi S, Sugimura K, Maruo T. Usefulness of Gd-DTPA contrast-enhanced dynamic MRI and serum determination of LDH and its isozymes in the differential diagnosis of leiomyosarcoma from degenerated leiomyoma of the uterus. Int. J. Gynecol. Cancer12,354-361 (2002).
18. Seki K, Hoshihara T, Nagata I. Leiomyosarcoma of the uterus, ultrasonography and serum lactate dehydrogenase level. Gynecol. Obstet. Invest.33,114-118 (1992).
19. Szabo I, Szantho A, Csabay L, Csapo Z, Szirmai K, Papp Z. Color doppler ultrasonography in the differentiation of uterine sarcomas from uterine leiomyomas. Eur. J. Gynaecol. Oncol.23,29-34 (2002).
20. Umesaki N, Tanaka T, Miyama M et al. Positron emission tomography with (18)-fluorodeoxyglucose of uterine sarcoma, a comparison with magnetic resonance imaging and power Doppler imaging. Gynecol. Oncol.80,372-377 (2001).
21. Vardi JR, Tovell HM. Leiomyosarcoma of the uterus, clinicopathologic study. Obstet. Gynecol.56,428-434 (1980).
22. Tanaka YO, Nishida M, Tsunoda H, Okamoto Y, Yoshikawa H. Smooth muscle tumors of uncertain malignant potential and leiomyosarcomas of the uterus, MR findings. J. Magn. Reson. Imaging.20,998-1007 (2004).
23. Al-Badr A, Faught W. Uterine artery embolization in an undiagnosed uterine sarcoma. Obstet. Gynecol.97,836-837 (2001).
24. Common AA, Mocarski EJ, Kolin A, Pron G, Soucie J. Therapeutic failure of uterine fibroid embolization caused by underlying leiomyosarcoma. J. Vasc. Interv. Radiol.12,1449-1452 (2001).
25. D’Angelo A, Amso NN, Wood A. Uterine leiomyosarcoma discovered after uterine artery embolisation. J. Obstet. Gynaecol.23,686-687 (2003).
26. Goldberg J, Burd I, Price FV, Worthington-Kirsch R. Leiomyosarcoma in a premenopausal patient after uterine artery embolization. Am. J. Obstet. Gynecol.191,1733-1735 (2004).
27. Joyce A, Hessami S, Heller D. Leiomyosarcoma after uterine artery embolization. A case report. J. Reprod. Med.46,278-280 (2001).
28. Papadia A, Salom EM, Fulcheri E, Ragni N. Uterine sarcoma occurring in a premenopausal patient after uterine artery embolization, a case report and review of the literature. Gynecol. Oncol.104,260-263 (2007).
29. Stohl Posy HE, Elkas JC, Yemelyanova AV, Diaz-Montes TP, Bristow RE, Giuntoli RL 2nd. Metastatic leiomyosarcoma diagnosed after uterine artery embolization. Eur. J. Gynaecol. Oncol.30,199-202 (2009).
30. Bell SW, Kempson RL, Hendrickson MR. Problematic uterine smooth muscle neoplasms. A clinicopathologic study of 213 cases. Am. J. Surg. Pathol.18,535-558 (1994).
31. Hendrickson MR, Kempson RL. Pure mesenchymal tumours of the uterine corpus. In: Haines and Taylor, Textbook of Obstetrical and Gynecolgical Pathology. Churchill Livingstone, Edinburgh, UK, 519 (1995).
32. Evans HL, Chawla SP, Simpson C, Finn KP. Smooth muscle neoplasms of the uterus other than ordinary leiomyoma. A study of 46 cases, with emphasis on diagnostic criteria and prognostic factors. Cancer62,2239-2247 (1988).
33. Fechner RE. Atypical leiomyomas and synthetic progestin therapy. Am. J. Clin. Pathol.49,697-703 (1968).
34. Burns B, Curry RH, Bell ME. Morphologic features of prognostic significance in uterine smooth muscle tumors, a review of eighty-four cases. Am. J. Obstet. Gynecol.135,109-114 (1979).
35. Hart WR, Billman JK Jr. A reassessment of uterine neoplasms originally diagnosed as leiomyosarcomas. Cancer41,1902-1910 (1978).
36. Wilkinson N, Rollason TP. Recent advances in the pathology of smooth muscle tumours of the uterus. Histopathology39,331-341 (2001).
37. Perrone T, Dehner LP. Prognostically favorable “mitotically active” smooth-muscle tumors of the uterus. A clinicopathologic study of ten cases. Am. J. Surg. Pathol.12,1-8 (1988).
38. Prayson RA, Hart WR Mitotically active leiomyomas of the uterus. Am. J. Clin. Pathol.97,14-20 (1992).
39. Kempson RL, Hendrickson MR. Smooth muscle, endometrial stromal, and mixed Mullerian tumors of the uterus. Mod. Pathol.13,328-342 (2000).
40. Rha SE, Byun JY, Jung SE et al. CT and MRI of uterine sarcomas and their mimickers. AJR Am. J. Roentgenol.181,1369-1374 (2003).
41. International Federation of Gynecology and Obstetrics. Annual report on the results of treatment in gynecologic cancer. Int. J. Gynecol. Obstet.28,189-190 (1989).
42. Lissoni A, Cormio G, Bonazzi C et al. Fertility-sparing surgery in uterine leiomyosarcoma. Gynecol. Oncol.70,348-350 (1998).
43. Kattan MW, Leung DH, Brennan MF. Postoperative nomogram for 12-year sarcoma-specific death. J. Clin. Oncol.20,791-796 (2002).
44. Lantta M, Karkkainen J, Wahlstrom T, Widholm O. Estradiol and progesterone receptors in gynecologic sarcomas. Acta Obstet. Gynecol. Scand.63,505-508 (1984).
45. Zhai YL, Kobayashi Y, Mori A et al. Expression of steroid receptors, Ki-67, and p53 in uterine leiomyosarcomas. Int. J. Gynecol. Pathol.18,20-28 (1999).
46. Abu-Rustum NR, Curtin JP, Burt M, Jones WB. Regression of uterine low-grade smooth-muscle tumors metastatic to the lung after oophorectomy. Obstet. Gynecol.89,850-852 (1997).
47. Nordal RR, Kristensen GB, Kaern J, Stenwig AE, Pettersen EO, Trope CG. The prognostic significance of stage, tumor size, cellular atypia and DNA ploidy in uterine leiomyosarcoma. Acta Oncol.34,797-802 (1995).
48. Leitao MM, Sonoda Y, Brennan MF, Barakat RR, Chi DS. Incidence of lymph node and ovarian metastases in leiomyosarcoma of the uterus. Gynecol. Oncol.91,209-212 (2003).
49. Berchuck A, Rubin SC, Hoskins WJ, Saigo PE, Pierce VK, Lewis JL Jr. Treatment of uterine leiomyosarcoma. Obstet. Gynecol.71,845-850 (1988).
50. Gadducci A, Landoni F, Sartori E et al. Uterine leiomyosarcoma, analysis of treatment failures and survival. Gynecol. Oncol.62,25-32 (1996).
51. Larson B, Silfversward C, Nilsson B, Pettersson F. Prognostic factors in uterine leiomyosarcoma. A clinical and histopathological study of 143 cases. The Radiumhemmet series 1936-1981. Acta Oncol.29,185-191 (1990).
52. Giuntoli RL 2nd, Metzinger DS, DiMarco CS et al. Retrospective review of 208 patients with leiomyosarcoma of the uterus, prognostic indicators, surgical management, and adjuvant therapy. Gynecol. Oncol.89,460-469 (2003).
53. Kapp DS, Shin JY, Chan JK. Prognostic factors and survival in 1396 patients with uterine leiomyosarcomas, emphasis on impact of lymphadenectomy and oophorectomy. Cancer112,820-830 (2008).
54. Goff BA, Rice LW, Fleischhacker D et al. Uterine leiomyosarcoma and endometrial stromal sarcoma, lymph node metastases and sites of recurrence. Gynecol. Oncol.50,105-109 (1993).
55. Bodner K, Bodner-Adler B, Kimberger O, Czerwenka K, Leodolter S, Mayerhofer K. Evaluating prognostic parameters in women with uterine leiomyosarcoma. A clinicopathologic study. J. Reprod. Med.48,95-100 (2003).
56. Hsieh CH, Lin H, Huang CC, Huang EY, Chang SY, Chang Chien CC. Leiomyosarcoma of the uterus, a clinicopathologic study of 21 cases. Acta Obstet. Gynecol. Scand.82,74-81 (2003).
57. Salazar OM, Dunne ME. The role of radiation therapy in the management of uterine sarcomas. Int. J. Radiat. Oncol. Biol. Phys.6,899-902 (1980).
58. Chauveinc L, Deniaud E, Plancher C et al. Uterine sarcomas, the Curie Institut experience. Prognosis factors and adjuvant treatments. Gynecol. Oncol.72,232-237 (1999).
59. Reed NS, Mangioni C, Malmstrom H et al. Phase III randomised study to evaluate the role of adjuvant pelvic radiotherapy in the treatment of uterine sarcomas stages I and II, an European Organisation for Research and Treatment of Cancer Gynaecological Cancer Group Study (protocol 55874). Eur. J. Cancer44,808-818 (2008).
60. Muss HB, Bundy BN, Adcock L, Beecham J. Mitoxantrone in the treatment of advanced uterine sarcoma. A Phase II trial of the Gynecologic Oncology Group. Am. J. Clin. Oncol.13,32-34 (1990).
61. Omura GA, Major FJ, Blessing JA et al. A randomized study of adriamycin with and without dimethyl triazenoimidazole carboxamide in advanced uterine sarcomas. Cancer52,626-632 (1983).
62. Sutton G, Blessing JA, Malfetano JH. Ifosfamide and doxorubicin in the treatment of advanced leiomyosarcomas of the uterus, a Gynecologic Oncology Group study. Gynecol. Oncol.62,226-229 (1996).
63. Omura GA, Blessing JA, Major F et al. A randomized clinical trial of adjuvant adriamycin in uterine sarcomas, a Gynecologic Oncology Group Study. J. Clin. Oncol.3,1240-1245 (1985).
64. Hensley ML, Blessing JA, Degeest K, Abulafia O, Rose PG, Homesley HD. Fixed-dose rate gemcitabine plus docetaxel as second-line therapy for metastatic uterine leiomyosarcoma, a Gynecologic Oncology Group Phase II study. Gynecol. Oncol.109,323-328 (2008).
65. Hensley ML, Blessing JA, Mannel R, Rose PG. Fixed-dose rate gemcitabine plus docetaxel as first-line therapy for metastatic uterine leiomyosarcoma, a Gynecologic Oncology Group Phase II trial. Gynecol. Oncol.109,329-334 (2008).
66. Hensley ML, Ishill N, Soslow R et al. Adjuvant gemcitabine plus docetaxel for completely resected stages I-IV high grade uterine leiomyosarcoma, Results of a prospective study. Gynecol. Oncol.112,563-567 (2009).
67. Herrero AB, Martin-Castellanos C, Marco E, Gago F, Moreno S. Cross-talk between nucleotide excision and homologous recombination DNA repair pathways in the mechanism of action of antitumor trabectedin. Cancer Res.66,8155-8162 (2006).
68. Amant F, Coosemans A, Renard V, Everaert E, Vergote I. Clinical outcome of ET-743 (Trabectedin Yondelis) in high-grade uterine sarcomas, report on five patients and a review of the literature. Int. J. Gynecol. Cancer19,245-248 (2009).
69. Gadducci A, Romanini A. Adjuvant chemotherapy in early stage uterine sarcomas, an open question. Eur. J. Gynaecol. Oncol.22,352-357 (2001).
70. Makker V, Abu-Rustum NR, Alektiar KM et al. A retrospective assessment of outcomes of chemotherapy-based versus radiation-only adjuvant treatment for completely resected stage I-IV uterine carcinosarcoma. Gynecol. Oncol.111,249-254 (2008).
71. Sutton G, Kauderer J, Carson LF, Lentz SS, Whitney CW, Gallion H. Adjuvant ifosfamide and cisplatin in patients with completely resected stage I or II carcinosarcomas (mixed mesodermal tumors) of the uterus, a Gynecologic Oncology Group study. Gynecol. Oncol.96,630-634 (2005).
72. Kushner DM, Webster KD, Belinson JL, Rybicki LA, Kennedy AW, Markman M. Safety and efficacy of adjuvant single-agent ifosfamide in uterine sarcoma. Gynecol. Oncol.78,221-227 (2000).
73. Peters WA 3rd, Howard DR, Andersen WA, Figge DC. Uterine smooth-muscle tumors of uncertain malignant potential. Obstet. Gynecol.83,1015-1020 (1994).
74. Leyvraz S, Zweifel M, Jundt G et al. Long-term results of a multicenter SAKK trial on high-dose ifosfamide and doxorubicin in advanced or metastatic gynecologic sarcomas. Ann. Oncol.17,646-651 (2006).
75. Sutton G, Blessing J, Hanjani P, Kramer P. Phase II evaluation of liposomal doxorubicin (Doxil) in recurrent or advanced leiomyosarcoma of the uterus, a Gynecologic Oncology Group study. Gynecol. Oncol.96,749-752 (2005).
76. Gallup DG, Blessing JA, Andersen W, Morgan MA. Evaluation of paclitaxel in previously treated leiomyosarcoma of the uterus, a gynecologic oncology group study. Gynecol. Oncol.89,48-51 (2003).
77. Sutton G, Blessing JA, Ball H. Phase II trial of paclitaxel in leiomyosarcoma of the uterus, a gynecologic oncology group study. Gynecol. Oncol.74,346-349 (1999).
78. Anderson S, Aghajanian C. Temozolomide in uterine leiomyosarcomas. Gynecol. Oncol.98,99-103 (2005).
79. Garcia del Muro X, Lopez-Pousa A, Martin J et al. A Phase II trial of temozolomide as a 6-week, continuous, oral schedule in patients with advanced soft tissue sarcoma, a study by the Spanish Group for Research on Sarcomas. Cancer104,1706-1712 (2005).
80. Anraku M, Yokoi K, Nakagawa K et al. Pulmonary metastases from uterine malignancies, results of surgical resection in 133 patients. J. Thorac. Cardiovasc. Surg.127,1107-1112 (2004).
81. Levenback C, Rubin SC, McCormack PM, Hoskins WJ, Atkinson EN, Lewis JL Jr. Resection of pulmonary metastases from uterine sarcomas. Gynecol. Oncol.45,202-205 (1992).
82. Leitao MM, Brennan MF, Hensley M et al. Surgical resection of pulmonary and extrapulmonary recurrences of uterine leiomyosarcoma. Gynecol. Oncol.87,287-294 (2002).
83. Giuntoli RL 2nd, Gostout BS, DiMarco CS, Metzinger DS, Keeney GL. Diagnostic criteria for uterine smooth muscle tumors, leiomyoma variants associated with malignant behavior. J. Reprod. Med.52,1001-1010 (2007).
84. Akhan SE, Yavuz E, Tecer A et al. The expression of Ki-67, p53, estrogen and progesterone receptors affecting survival in uterine leiomyosarcomas. A clinicopathologic study. Gynecol. Oncol.99,36-42 (2005).
85. Hardman MP, Roman JJ, Burnett AF, Santin AD. Metastatic uterine leiomyosarcoma regression using an aromatase inhibitor. Obstet. Gynecol.110,518-520 (2007).
86. Quek R, George S. Gastrointestinal stromal tumor, a clinical overview. Hematol. Oncol. Clin. North Am.23,69-78 (2009).
87. Wang L, Felix JC, Lee JL et al. The proto-oncogene c-kit is expressed in leiomyosarcomas of the uterus. Gynecol. Oncol.90,402-406 (2003).
88. Winter WE 3rd, Seidman JD, Krivak TC et al. Clinicopathological analysis of c-kit expression in carcinosarcomas and leiomyosarcomas of the uterine corpus. Gynecol. Oncol.91,3-8 (2003).
89. Rushing RS, Shajahan S, Chendil D et al. Uterine sarcomas express KIT protein but lack mutation(s) in exon 11 or 17 of c-KIT. Gynecol. Oncol.91,9-14 (2003).
90. Raspollini MR, Amunni G, Villanucci A et al. c-Kit expression in patients with uterine leiomyosarcomas, a potential alternative therapeutic treatment. Clin. Cancer Res.10,3500-3503 (2004).
91. Serrano C, Mackintosh C, Herrero D et al. Imatinib is not a potential alternative treatment for uterine leiomyosarcoma. Clin. Cancer Res.11,4977-4980 (2005).
92. Bodner-Adler B, Bodner K, Kimberger O, Czerwenka K, Leodolter S, Mayerhofer K. MMP-1 and MMP-2 expression in uterine leiomyosarcoma and correlation with different clinicopathologic parameters. J. Soc. Gynecol. Investig.10,443-446 (2003).
93. Atkins KA, Arronte N, Darus CJ, Rice LW. The use of p16 in enhancing the histologic classification of uterine smooth muscle tumors. Am. J. Surg. Pathol.32,98-102 (2008).
94. Skubitz KM, Pambuccian S, Manivel JC, Skubitz AP. Identification of heterogeneity among soft tissue sarcomas by gene expression profiles from different tumors. J. Transl. Med.6,23 (2008).
95. Skubitz KM, Skubitz AP. Differential gene expression in leiomyosarcoma. Cancer98,1029-1038 (2003).